고려대 연구팀, 헤모글로빈 전환 조절 핵심 인자 LDB1 규명
한국연구재단은 23일 전태훈 고려대학교 의과대학 교수 연구팀이 적혈구가 자라는 과정에서 헤모글로빈 종류를 바꾸는 '헤모글로빈 전환(hemoglobin switching)'을 조절하는 핵심 단백질 LDB1의 역할을 규명했다고 밝혔다.
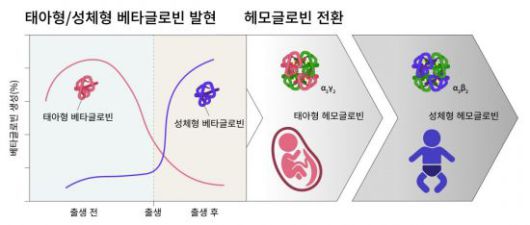 |
포유류 적혈구 분화 과정에서 태아형 헤모글로빈(HbF, α₂γ₂)이 출생 후 성체형 헤모글로빈(HbA, α₂β₂)으로 전환되는 과정을 나타낸 모식도. 성체 단계에서는 BCL11A, CBFA2T3, SOX6 등이 γ-globin 발현을 억제해 전환을 유도한다. 그림 제공 및 설명 : 고려대학교 전태훈 교수. |
<이미지를 클릭하시면 크게 보실 수 있습니다> |
헤모글로빈 전환은 태아기에서 성체기로 성장하는 과정에서 혈색소의 종류가 바뀌는 현상이다. 이 과정이 제대로 이뤄지지 않으면 성체형 헤모글로빈 생성이 감소해 베타-지중해빈혈(β-thalassemia)과 같은 유전성 빈혈이 발생한다. 하지만 그동안 이를 통합적으로 조절하는 '상위 인자'는 명확히 밝혀지지 않았다.
연구팀은 적혈구 전구세포에서 LDB1 단백질이 선택적으로 결핍된 생쥐 모델을 제작해 LDB1이 태아형 헤모글로빈을 억제하는 유전자의 발현을 직접 촉진하는 전사 활성화 인자라는 사실을 확인했다.
실험 결과 LDB1이 결핍된 세포에서는 BCL11A, CBFA2T3, SOX6 등 태아형 헤모글로빈 억제 유전자의 발현이 크게 감소했고, 태아형 헤모글로빈은 50배 이상 과도하게 증가했다. 동시에 활성산소(ROS)가 약 10배 상승하면서 적혈구 전구세포의 세포자살이 유도됐고, 정상적인 적혈구 분화가 이뤄지지 않았다.
실제로 LDB1 결핍 생쥐는 적혈구 수가 정상 대비 10% 이하로 감소했고, 출생 후 7일 이내 모두 사망했다. 이는 베타-지중해빈혈 환자에서 관찰되는 조혈 장애와 유사한 병태생리를 재현한 것이다.
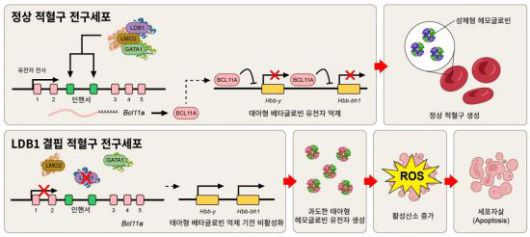 |
정상과 Ldb1 결핍 적혈구 전구세포의 분화 과정 비교. LDB1이 결핍되면 Bcl11a 등 억제 유전자 발현이 감소해 태아형 헤모글로빈이 과도하게 유지되고, 활성산소 증가와 세포자살로 인해 적혈구 성숙이 중단된다. 그림 제공 및 설명 : 고려대학교 전태훈 교수. |
<이미지를 클릭하시면 크게 보실 수 있습니다> |
이번 연구의 핵심은 LDB1이 단순한 보조 단백질이 아니라, BCL11A 등 여러 핵심 유전자를 동시에 조절하는 '상위 조절자'라는 점을 입증했다는 데 있다. 기존 치료 전략이 단일 유전자 표적에 집중해왔다면, 이번 연구는 헤모글로빈 전환을 통합적으로 제어할 수 있는 경로를 제시했다는 의미다.
전태훈 교수는 "LDB1이 태아형에서 성체형으로의 헤모글로빈 전환을 주도하는 핵심 조절 인자임을 확인했다"며 "현재 베타-지중해빈혈 치료에 사용되는 유전자 편집 치료제 '카스게비(Casgevy)'의 주요 표적 유전자인 BCL11A를 포함해 여러 전환 관련 유전자를 동시에 조절하는 차세대 치료 전략으로 확장될 수 있다"고 말했다.
Casgevy는 크리스퍼-카스9(CRISPR-Cas9) 기반 유전자 편집 기술을 이용해 개발된 세계 최초의 유전자 편집 치료제로, 2023년 미국 식품의약국(FDA)과 영국 의약품건강관리제품규제청(MHRA) 승인을 받았다. 단 한 번의 치료로 평생 수혈을 대체할 수 있는 혁신 치료제로 평가받지만, 단일 유전자 표적 중심이라는 한계도 지닌다.
연구 성과는 과학기술정보통신부와 한국연구재단이 추진하는 중견연구 사업의 지원으로 수행됐으며, 생화학·분자생물학 분야 국제학술지 Redox Biology에 지난 4일 온라인 게재됐다.
연구팀은 LDB1 결핍 생쥐 모델이 베타-지중해빈혈과 사립체성 빈혈(sideroblastic anemia) 등 산화 스트레스 관련 혈액 질환 연구와 치료제 효능 평가를 위한 전임상 모델로 활용될 수 있을 것으로 보고 있다.
이번 연구는 난치성 유전성 빈혈 치료 전략을 '단일 유전자 편집'에서 '상위 전사 조절 경로 조절'로 확장할 수 있는 가능성을 제시했다는 점에서 학계의 주목을 받고 있다.
김종화 기자 justin@asiae.co.kr
<ⓒ투자가를 위한 경제콘텐츠 플랫폼, 아시아경제(www.asiae.co.kr) 무단전재 배포금지>
이 기사의 카테고리는 언론사의 분류를 따릅니다.
기사가 속한 카테고리는 언론사가 분류합니다.
언론사는 한 기사를 두 개 이상의 카테고리로 분류할 수 있습니다.
언론사는 한 기사를 두 개 이상의 카테고리로 분류할 수 있습니다.


