KIST 연구팀, 비정상적 타우 단백질 응집 초기단계부터 관찰할 수 있는 동물모델 개발
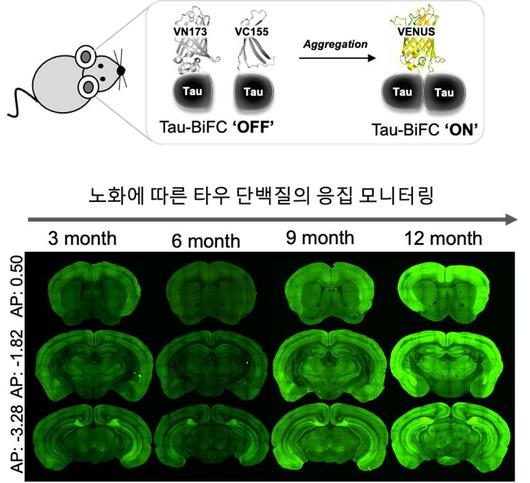 |
타우-BiFC 생쥐모델의 뇌에서 노화에 따른 타우 응집 정도 모니터링.[KIST 제공] |
<이미지를 클릭하시면 크게 보실 수 있습니다> |
[헤럴드경제=구본혁 기자] 머릿속 치매 원인물질을 초기 단계부터 정밀 관찰할 수 있는 새로운 치매 플랫폼 기술이 국내 연구진에 의해 개발됐다.
한국과학기술연구원(KIST) 치매DTC융합연구단 김윤경·임성수 박사 연구팀은 치매 유발 원인으로 알려진 타우 단백질의 응집을 초기 단계부터 관찰할 수 있는 동물 모델을 개발했다고 21일 밝혔다. 이 신규 플랫폼을 활용하면 치료제 개발 연구를 가속화하고, 새로운 치매 기전을 규명할 수 있을 것으로 기대된다.
가장 흔한 퇴행성 뇌 질환인 알츠하이머성 치매는 뇌 속 베타-아밀로이드 단백질이나 타우 단백질이 응집되는 것이 주요 원인으로 여겨지고 있다. 베타-아밀로이드 응집은 뇌 기능이 손상되는 데에 길게는 10년 이상이 걸리기도 하며 심지어 병변이 나타나지 않는 때도 있다.
타우 단백질이 응집되기 시작하면 단백질이 뭉친 형태인 올리고머 형태가 되는데, 이는 신경세포 독성을 일으키고 알츠하이머성 치매를 비롯한 다양한 퇴행성 뇌 질환을 전이시키는 매개체로 작용한다. 이에 타우 올리고머를 표적으로 한 치매 치료제 개발이 화두에 오르고 있지만, 신경세포 내 과량으로 존재하는 정상 타우 단백질로부터 응집 초기에 소량으로 존재하는 타우 올리고머를 구분해낼 실험 방법은 없었다.
연구팀은 세포에서 타우 올리고머의 형성을 관찰할 수 있는 플랫폼인 ‘타우-BiFC 플랫폼’을 확립하고 이를 동물 모델로 확장한 ‘타우-BiFC 생쥐 모델’을 개발했다. 이 플랫폼은 신경세포 내에서 타우 단백질이 응집해 올리고머가 형성되면 형광이 켜지는 시스템으로 타우 응집 초기 올리고머 단계부터 정량적으로 관찰할 수 있다는 장점이 있다.
연구팀이 개발한 ‘타우-BiFC 생쥐’를 통해 단계별로 정량적인 모니터링이 가능했다. 생쥐가 어린 나이일 때 타우 올리고머가 생성돼도 세포 자체적으로 분해·제거하는 시스템이 가동되지만, 생쥐가 나이가 들수록 그 기능이 떨어져 타우의 응집이 가속되고 신경이 퇴화하는 특성을 보이는 것을 관찰할 수 있었다.
김윤경 박사는 “이번 기술 개발로 외국에서 개발된 생쥐 모델에 의존하던 기존 치매 연구를 탈피할 수 있을 것”이라며 “신경세포 독성 및 전이성을 보이는 타우 응집체의 형성을 파악하고 관찰하는 연구는 알츠하이머성 치매를 포함한 타우 병증 치료제 개발에 있어 중요한 시작점이라 할 수 있다”고 말했다.
이번 연구 성과는 신경과학 분야 국제학술지 ‘Progress in Neurobiology’ 최신호에 게재됐다.
nbgkoo@heraldcorp.com
- Copyrights ⓒ 헤럴드경제 & heraldbiz.com, 무단 전재 및 재배포 금지 -
이 기사의 카테고리는 언론사의 분류를 따릅니다.
기사가 속한 카테고리는 언론사가 분류합니다.
언론사는 한 기사를 두 개 이상의 카테고리로 분류할 수 있습니다.
언론사는 한 기사를 두 개 이상의 카테고리로 분류할 수 있습니다.


