WHO선 “효과 없다” 밝혀 논란
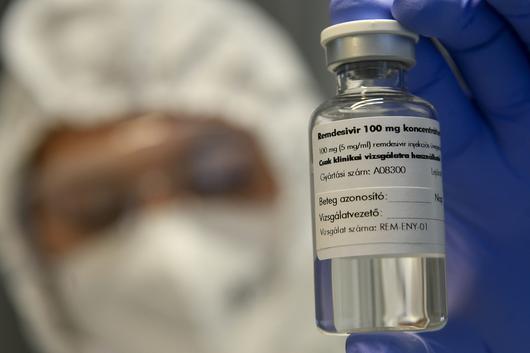 |
/AP 연합뉴스 |
<이미지를 클릭하시면 크게 보실 수 있습니다> |
미 식품의약국(FDA)은 22일(현지 시각) 미국 제약사 길리어드사이언스의 항바이러스제 렘데시비르를 코로나 입원 환자에 대한 치료제로 정식 승인했다. 렘데시비르는 미국 정부가 코로나 치료제로 정식 허가한 유일한 의약품이 됐다. 당초 에볼라 치료제로 주목받았던 렘데시비르는 지난 5월 FDA 긴급 사용 승인을 받아 코로나 치료제로 사용돼 왔다. 도널드 트럼프 미 대통령도 코로나 치료 과정에서 렘데시비르를 투여받은 바 있다.
FDA는 일단 코로나로 입원이 필요한 환자 중 성인과 12세 이상(체중 40kg 이상)에게만 렘데시비르 사용이 가능하다고 전했다. 스티븐 한 FDA 국장은 “이번 승인은 FDA가 엄격하게 평가한 여러 임상시험 자료가 바탕이 됐다”고 했다. FDA는 렘데시비르 투여 환자 그룹의 회복 기간이 투여하지 않은 환자 그룹보다 5일 더 짧았다는 미 국립알레르기·감염병연구소의 임상시험 결과를 전하기도 했다.
그러나 앞서 세계보건기구(WHO)는 입원 환자 1만1266명을 상대로 진행한 다국적 임상시험에서 렘데시비르가 환자의 입원 기간을 줄이거나 사망률을 낮추지 못했다고 밝힌 바 있다. 이 때문에 렘데시비르 정식 승인에 대한 미국 내 논란이 여전하다. 뉴욕타임스는 “트럼프 대통령이 코로나 치료제를 약속해온 상황에서, 렘데시비르는 대선일을 2주도 채 남기지 않은 시점에 승인을 받았다”고 보도했다.
[이옥진 기자]
- Copyrights ⓒ 조선일보 & chosun.com, 무단 전재 및 재배포 금지 -
이 기사의 카테고리는 언론사의 분류를 따릅니다.
기사가 속한 카테고리는 언론사가 분류합니다.
언론사는 한 기사를 두 개 이상의 카테고리로 분류할 수 있습니다.
언론사는 한 기사를 두 개 이상의 카테고리로 분류할 수 있습니다.


