 |
코로나19 신규 확진자가 11만 9603명 발생, 엿새 연속 10만명대를 기록한 14일 서울역 광장 임시선별검사소에서 시민들과 해외에서 입국한 여행객들이 검체 검사를 위해 줄을 서 있다. 이날 위중증 환자는 512명으로, 107일 만에 가장 많은 것으로 집계됐다. /성동훈 기자 |
<이미지를 클릭하시면 크게 보실 수 있습니다> |
코로나19 유행 규모가 커진 여파로 위중증 환자와 사망자 수가 급증하고 있다. 당국은 4차 백신 접종이 더딘 상황에서 중증화율을 낮추기 위해 먹는 치료제 처방률을 높이는 데 집중하고 있다. 또 해외에서 개발한 신규 치료제 사용 여부를 따져보기 위한 검토에 들어갔다.
14일 질병관리청 중앙방역대책본부(방대본)에 따르면 이날 0시 기준 신규 확진자는 11만9603명으로 일주일 전인 지난 7일(10만5507명)보다 1.13배 늘었다. 위중증 환자 수는 500명대(512명)로 늘며 지난 4월29일(526명) 이후 107일 만에 최다 수준이다. 사망자는 57명이다. 중증 병상 가동률은 42.5%, 준중증 병상 가동률은 62.1%다. 당국은 병상 가동률이 ‘70%’를 넘어서면 위험신호로 본다.
지난 10일 기준 국가수리과학연구소의 수리모델링 분석에 따르면 연구팀들은 이달 말 20만명 중반부터 많게는 30만명 규모의 확진자가 발생할 것으로 예상했다. 확진자가 늘면 위중증 환자도 늘 수밖에 없는데, 4차 접종률은 지난 12일 기준 12.6%(60세 이상 40.2%)에 그친다.
‘먹는 치료제’ 처방률 제고 관건
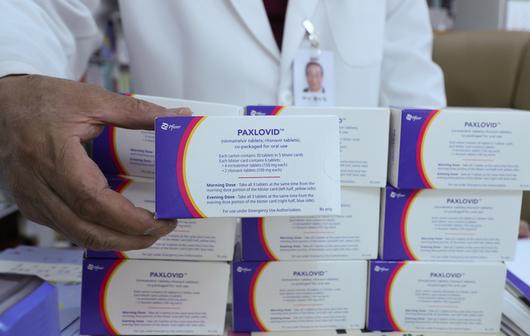 |
팍스로비드. 연합뉴스 |
<이미지를 클릭하시면 크게 보실 수 있습니다> |
정부가 표방하는 ‘표적방역’의 핵심 중 하나는 ‘먹는 치료제’다. 경증 환자에 적기에 투여해 중증화율을 낮출 수 있기 때문이다. 정부는 지난 12일 먹는 치료제 처방 기관을 현재 동네 병·의원 중심 원스톱진료기관에서 종합병원까지 대폭 확대하고 조제가 가능한 약국도 기존 1082곳에서 2175곳으로 늘린다는 구상을 밝혔다. 다만 정부가 처방·조제기관을 지정하는 게 아니라, 신청을 받기 때문에 의약기관의 협조를 얻어내는 게 관건이다. 팍스로비드는 병용금지 의약품이 23개나 되기 때문에 의료진이 처방하기 까다롭다는 의견이 많다. 이에 정부는 의료진 대상 임상 정보 공유 및 교육도 강화하기로 했다.
국내서 쓰이는 먹는 치료제는 팍스로비드와 라게브리오로, 60세 이상 환자와 12세 이상(팍스로비드) 또는 18세 이상(라게브리오) 기저질환자와 면역저하자 등이 투여 대상이다. 현재 60세 이상 확진자의 먹는 치료제 평균 투여율은 18%대에 머물고 있다.
질병청에 따르면 지난 13일 기준으로 국내 도입된 106만2000명분(팍스로비드 96.2만명분, 라게브리오 10만명분) 중 38만8000명분을 썼다. 재고가 67만5000명분인데 이 중 팍스로비드 61만3000명분의 사용기한은 내년 2월까지라 다수를 폐기처분할 수도 있다는 지적이 나온다. 질병청은 지난 13일 설명자료에서 “현재 팍스로비드 최근 1주일(5~11일) 일평균 사용량 기준(약 5000명분)으로 추계하였을 때 11월까지 사용 가능한 물량”이라고 설명했다. 질병청은 또 팍스로비드 사용기간을 6개월 연장하는 안도 제약사와 협의하고 있다고 덧붙였다.
질병청은 하반기 먹는 치료제 수요가 늘 것으로 보고 팍스로비드 80만명분, 라게브리오 14만2000명을 추가 도입하기로 하고 구매 계약을 맺었고, 오는 8~9월에 라게브리오 물량이 우선 도입될 예정이라고 밝혔다.
신규 치료제 ‘사비자불린’은 어떤 치료제
식품의약품안전처는 지난 12일 미국 제약사 베루(Veru)가 개발한 먹는 코로나19 치료제(성분명 사비자불린·Sabizabulin)에 대한 사전검토에 착수했다고 밝혔다.
식약처에 따르면 사비자불린은 바이러스가 세포 내에서 증식하는 데 필요한 미세소관 생성을 저해해 바이러스 복제와 염증 작용을 억제한다. 베루는 지난달 6일 미국 식품의약국(FDA)에 긴급사용허가 요청서를 제출했고, 유럽의약품청(EMA)도 지난달 28일 사비자불린 사용 검토에 들어갔다.
사비자불린은 본래 항암제로 개발됐다. 팍스로비드와 라게브리오가 경증 환자에 쓰이는 치료제인 반면 사비자불린은 중증 환자를 대상으로 한다. 지난달 6일 국제 학술지 뉴잉글랜드저널오브메디신(NEJM)에 실린 임상 3상 연구결과에 따르면 중증 환자 204명을 대상으로 한 실험에서 위약 대비 사비자불린의 상대적인 사망 위험도는 55.2% 수준으로 감소한 것으로 나타났다.
그러나 사비자불린 임상 참여자가 수가 204명으로 매우 적기 때문에 임상 연구 결과 해석에 주의해야 한다는 의견도 있다. 데이비드 보울웨어 미 미네소타대 의대 교수는 지난달 6일 뉴욕타임스에 “위약그룹에서 사망자률은 다소 높게 나타났다. 실험 참가자 수가 적어서 (효과에 대해) 확실한 결론을 낼 수 없다는 것을 의미할 수 있다”며 팍스로비드와 라게브리오의 효과가 임상 연구 결과보다 실제 의료현장 사용 시에 줄어든 것처럼 사비자불린의 임상 연구결과에 대해서도 회의적이라고 밝혔다.
김향미 기자 sokhm@kyunghyang.com
▶ [뉴스레터]좋은 식습관을 만드는 맛있는 정보
▶ ‘눈에 띄는 경제’와 함께 경제 상식을 레벨 업 해보세요!
©경향신문(www.khan.co.kr), 무단전재 및 재배포 금지
이 기사의 카테고리는 언론사의 분류를 따릅니다.
기사가 속한 카테고리는 언론사가 분류합니다.
언론사는 한 기사를 두 개 이상의 카테고리로 분류할 수 있습니다.
언론사는 한 기사를 두 개 이상의 카테고리로 분류할 수 있습니다.


