 |
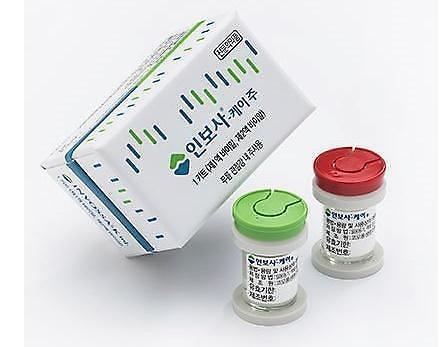
골관절염 치료제 인보사케이주 |
골관절염 치료제인 '인보사케이주(인보사)' 허가를 받기 위해 허위 자료를 제출한 혐의로 재판에 넘겨진 코오롱생명과학 임원들에게 1심에서 무죄가 선고됐다.
서울중앙지방법원 형사합의 25-3부(권성수·임정엽·김선희 부장판사)는 19일 위계공무집행방해·특정경제범죄 가중처벌법상 사기·보조금법 위반 등 혐의를 받는 임원 조모씨와 김모씨에게 무죄를 선고했다.
다만 조씨는 인보사 개발 과정에서 편의를 제공해달라는 청탁과 함께 식품의약품안전처 공무원에게 약 200만 원을 건넨 혐의(뇌물공여)만 유죄로 인정돼 벌금 500만원이 내려졌다.
임상개발팀장으로서 개발을 총괄했던 조씨와 바이오신약연구소장이었던 김씨는 식약처 허가를 받기 위해 인보사 성분에 대한 허위 자료를 제출한 혐의로 기소됐다.
재판부는 대법원 판례를 바탕으로 임원들이 자료를 허위로 제출한 것이 문제가 아니라 식약처가 사실 확인을 제대로 하지 않은 점이 문제라고 판단했다.
재판부는 "식약처는 인보사 세포와 관련해서 충실한 입증을 요구할 기회가 있던 것으로 보여진다"며 "식약처 태도는 단순히 개발사가 더 신뢰도가 높은 특별한 방법이 없다고 주장하는 것만으로 추가적인 다른 요구를 하지 않은 것으로 보인다"고 했다.
재판부는 이들이 일부 사실에 부합하지 않는 내용을 자료에 기재했다고 인정하면서도 "인보사 품목 허가 과정에서 식약처 검증이 부족한 것이 아닌지 의심된다"고 지적했다. 허위 서류 여부를 식약처가 주도적으로 검증했어야 한다는 취지다.
그러면서 "식약처가 종양원성 특성 정보 파악하는데 충분한 심성 다했는지 합리적 의심 여지없이 증명됐다고 보기 어렵다"며 무죄 판결을 내렸다.
인보사는 사람 연골에서 추출한 연골세포(1액)와 연골세포 성장인자(TGF-β1)를 도입한 형질전환세포(2액)로 구성된 골관절염 유전자치료제 주사액이다. 2017년 7월 국내 첫 유전자약으로 식약처 허가를 받았다. 그간 투약한 환자만 3700여명에 달한다.
그러나 2액에 든 형질전환세포가 허가 당시 신고한 연골세포가 아닌 종양을 유발할 수 있는 신장세포로 드러나 지난 5월 식약처가 허가를 취소하고 검찰에 고발했다.
김태현 기자 taehyun13@ajunews.com
- Copyright ⓒ [아주경제 ajunews.com] 무단전재 배포금지 -
이 기사의 카테고리는 언론사의 분류를 따릅니다.
기사가 속한 카테고리는 언론사가 분류합니다.
언론사는 한 기사를 두 개 이상의 카테고리로 분류할 수 있습니다.
언론사는 한 기사를 두 개 이상의 카테고리로 분류할 수 있습니다.