식약처, 가이드라인 개정‧‧‧최신 국제기준 'ISO 14971' 적용
 |
[출처 : 123RF.com] |
<이미지를 클릭하시면 크게 보실 수 있습니다> |
[출처 : 123RF.com]의료기기의 설계부터 생산‧사용까지 모든 과정에서 발생하는 위험을 보다 철저하게 관리할 수 있는 새로운 기준이 나왔다.
식품의약품안전처는 국내 의료기기 업계의 제조‧품질관리 수준을 높이기 위해서 최신 글로벌 기준인 'ISO 14971’을 반영한 '의료기기 위험 관리 가이드라인’을 24일 개정했다고 밝혔다.
식약처는 "이번 가이드라인 개정이 의료기기 위험 관리에 대한 업계 이해도를 높이는데 도움이 될 것으로 기대한다"며 "앞으로도 글로벌 규제 조화를 통해서 안전한 의료기기 공급에 필요한 지원을 지속해 나가겠다"고 말했다.
'위험 관리(Risk Mangement)’는 위험을 분석하고 평가‧모니터링하는 업무에 대한 관리 정책 및 절차 등을 체계적으로 적용하는 프로세스다.
가이드라인의 개정 내용은 글로벌 의료기기 위험분석 가이드라인(ISO 14971)의 개정 사항인 △의료기기 위험 관리 절차의 각 단계별 해설 △의료기기 위험 통제 방법 △의료기기 생산 후 정보수집 및 활용 방법 △의료기기 위험분석 기법 반영 등을 담았다.
'의료기기 위험 관리 절차’는 '위험분석 → 위험평가 → 위험통제 → 전체 잔여위험 평가 → 검토 → 생산 및 생산 후 활동’으로 구분한다.
'의료기기 위험 통제’는 위험을 규정된 수준 이하로 감소시키거나 유지토록 결정하고 조치가 수행되는 프로세스다.
특히 이번 가이드라인에선 의료기기와 관련된 모든 과정에서 발생할 수 있는 위험에 대한 분석‧평가‧관리 방법을 해설과 함께 구체적인 사례도 담아, 제조 현장의 활용도를 높였다.
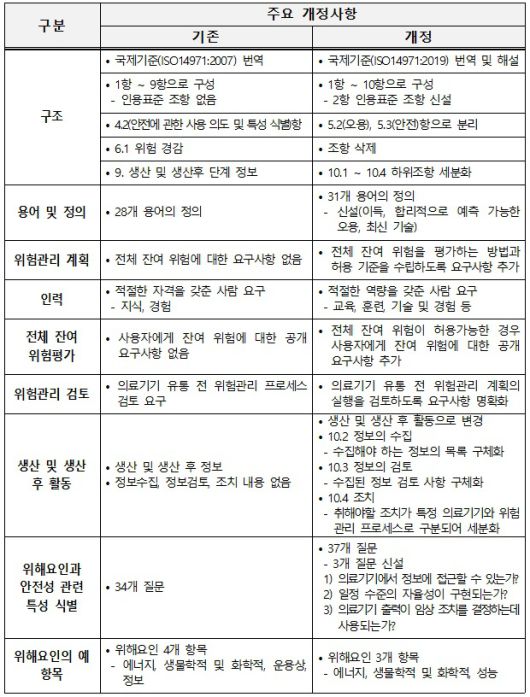 |
주요 가이드라인 개정 내용 |
<이미지를 클릭하시면 크게 보실 수 있습니다> |
주요 가이드라인 개정 내용
<저작권자 Copyright ⓒ 힐팁 무단전재 및 재배포 금지>
이 기사의 카테고리는 언론사의 분류를 따릅니다.
기사가 속한 카테고리는 언론사가 분류합니다.
언론사는 한 기사를 두 개 이상의 카테고리로 분류할 수 있습니다.
언론사는 한 기사를 두 개 이상의 카테고리로 분류할 수 있습니다.


